Casimersen (AMONDYS 45™) is a therapeutic antisense oligonucleotide designed for patients with Duchenne Muscular Dystrophy (DMD) whose gene mutation is amenable to exon 45 skipping. DMD is a genetic disorder characterized by the absence of dystrophin, a crucial protein for muscle function. This results in progressive muscle degeneration and loss of mobility, eventually affecting the heart and lungs. Casimersen works by binding to the mutated pre-mRNA, skipping exon 45 to allow the production of a functional, albeit shorter, dystrophin protein, which helps stabilize muscle integrity.
The drug was approved by the FDA in February 2021 under the accelerated approval program due to its demonstrated ability to increase dystrophin levels in treated patients. While the drug offers hope for managing the disease, it is not a cure. Casimersen is currently undergoing Phase III clinical trials to confirm its long-term benefits and assess its broader clinical implications.
In the ESSENCE trial, patients receiving Casimersen showed a statistically significant increase in dystrophin levels compared to the placebo group. This result supports its potential as a key therapy for DMD patients with exon 45 mutations. Casimersen's most common side effects were mild, including upper respiratory tract infections and headaches.
Although the drug's efficacy has been proven, monitoring for long-term adverse effects, particularly regarding kidney function, is ongoing. Despite its limitations, Casimersen is an important step toward treating about 8% of DMD patients whose mutations are amenable to exon 45 skipping.
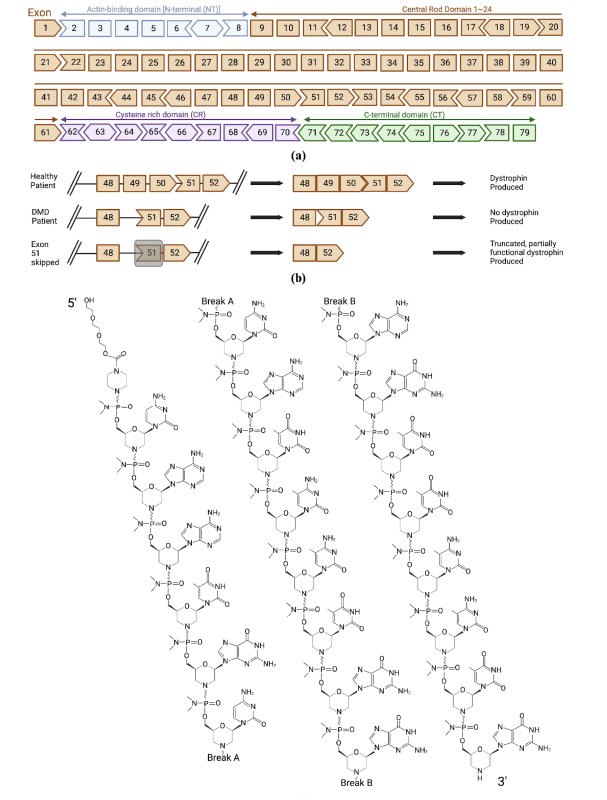
کاسیمرسن (AMONDYS 45™) یک الیگونوکلئوتید آنتیسنس است که برای بیماران مبتلا به دیستروفی عضلانی دوشن (DMD) که دارای جهش در ژن DMD و قابل حذف اگزون 45 هستند، طراحی شده است. دیستروفی عضلانی دوشن یک اختلال ژنتیکی است که به دلیل نبود پروتئین دیستروفین، باعث تخریب پیشرونده عضلات میشود. کاسیمرسن با اتصال به پیش-mRNA جهش یافته، از اگزون 45 عبور کرده و باعث تولید یک پروتئین دیستروفین عملکردی و کوتاه میشود که به تثبیت ساختار عضلات کمک میکند. این دارو در فوریه 2021 توسط FDA تحت برنامه تایید سریع تصویب شد، زیرا توانایی آن در افزایش سطح دیستروفین در بیماران تحت درمان نشان داده شده بود. اگرچه این دارو امیدی برای کنترل بیماری ایجاد میکند، اما درمان قطعی نیست. کاسیمرسن در حال حاضر در مرحله سوم کارآزماییهای بالینی برای تایید فواید بلندمدت و ارزیابی نتایج گستردهتر است. در کارآزمایی ESSENCE، بیماران تحت درمان با کاسیمرسن افزایش معنیداری در سطح دیستروفین نسبت به گروه دارونما نشان دادند. این نتایج از پتانسیل این دارو بهعنوان یک درمان کلیدی برای بیماران DMD با جهشهای اگزون 45 پشتیبانی میکند. عوارض جانبی کاسیمرسن عموماً خفیف بوده و شامل عفونتهای دستگاه تنفسی فوقانی و سردرد بوده است. در حالی که اثربخشی دارو اثبات شده است، نظارت بر عوارض جانبی بلندمدت، به ویژه در عملکرد کلیهها، همچنان ادامه دارد. علیرغم محدودیتها، کاسیمرسن گامی مهم برای درمان حدود 8 درصد از بیماران DMD است که جهش آنها قابل حذف اگزون 45 است.

| Information | Details |
| Authors | Milyard Assefa, Addison Gepfert, Meesam Zaheer, Julia M. Hum, Brian W. Skinner |
| Corresponding Author | Julia M. Hum |
| Article Title | Casimersen (AMONDYS 45™): An Antisense Oligonucleotide for Duchenne Muscular Dystrophy |
| Publication Date | 20-Apr-24 |
| Journal Name | Biomedicines |
| Keywords | AMONDYS 45, antisense oligonucleotide, casimersen, Duchenne muscular dystrophy, dystrophin |
| Methods Used | Exon skipping, clinical trials (Phase III), dystrophin quantification, immunofluorescence |
| DOI | 10.3390/biomedicines12040912 |