Exon Skipping: A Potential Treatment for Genetic Disorders
This article is simplified from English Wikipedia.
Source: Exon Skipping - Wikipedia
Exon skipping is a molecular biology technique used to address genetic mutations by causing cells to bypass defective sections (exons) of the genetic code. This process involves manipulating RNA splicing, specifically targeting mutations in the pre-messenger RNA.
How Exon Skipping Works
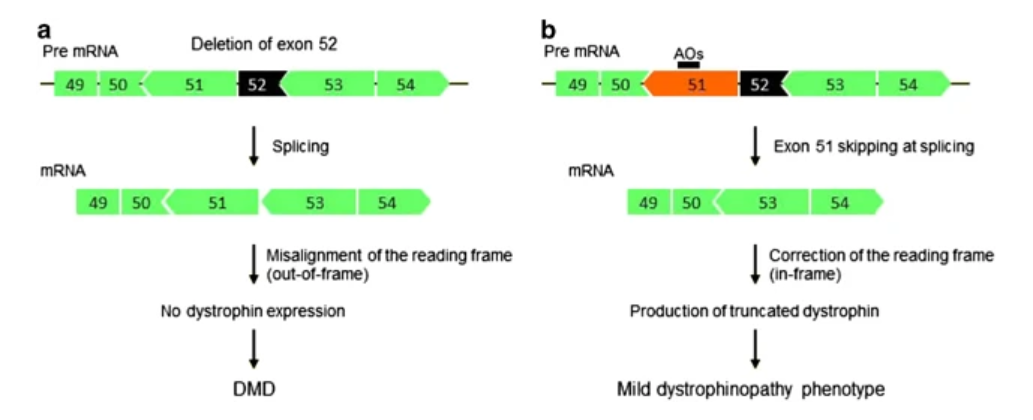
Genes contain coding regions called exons, which provide instructions for protein creation, separated by non-coding introns. Exon skipping aims to restore the reading frame within a gene by using antisense oligonucleotides (AONs), short synthetic molecules. These AONs bind to mutated exons, allowing the cell to skip over them during translation, thereby restoring the disrupted reading frame and producing a functional protein.
Exon Skipping and Duchenne Muscular Dystrophy (DMD)
This technique is actively researched for treating Duchenne muscular dystrophy (DMD), a condition where the dystrophin protein is prematurely truncated, leading to a non-functional protein. Exon skipping could potentially result in a mostly functional dystrophin protein, resembling a less severe form of muscular dystrophy.
Mechanism of Action in DMD
In the case of DMD, exon skipping targets mutations in the central rod domain of the dystrophin gene. By inducing the deletion of specific exons within this domain, exon skipping aims to convert a severe DMD mutation into a less harmful form, similar to Becker muscular dystrophy. Becker muscular dystrophy is associated with in-frame deletions, allowing for a shorter dystrophin protein that retains functionality.
FDA-Approved Exon Skipping Drugs
Several exon-skipping drugs, such as Eteplirsen, Golodirsen, and Viltolarsen, have been approved for DMD treatment by the U.S. FDA. These drugs target specific exons and have shown promise in addressing the genetic mutations causing DMD. Genetic testing can determine the nature and location of DMD mutations, with a focus on 'hot spot' regions, potentially allowing exon skipping to benefit up to 50% of DMD patients.