روشی نوین برای رساندن ژندرمانی مستقیماً به عضله:
ویروسهای مهندسیشده که تنها سلولهای عضلانی را هدف میگیرند
بیماریهای عضلانی مانند دیستروفی عضلانی دوشن (DMD) از جمله اختلالات جدی هستند که به مرور زمان باعث ضعف و تحلیل عضلات میشوند. بسیاری از این بیماریها، ژنتیکی هستند؛ یعنی به دلیل وجود نقص در یک ژن حیاتی برای عملکرد طبیعی عضله ایجاد میشوند. برای مثال، در بیماری دوشن، ژنی که مسئول تولید پروتئین دیستروفین است دچار نقص شده و بدون این پروتئین، عضلات بهمرور تخریب میشوند.
ژندرمانی یک روش نویدبخش برای درمان چنین بیماریهایی است. در این روش، نسخهای سالم از ژن معیوب به سلولهای عضلانی منتقل میشود تا آنها بتوانند پروتئین مورد نیاز خود را تولید کرده و از پیشرفت بیماری جلوگیری کنند.
اما رساندن ژن بهطور اختصاصی به سلولهای عضلانی کار آسانی نیست. یکی از چالشهای بزرگ در ژندرمانی این است که ژن مورد نظر باید در مکان درست، در زمان مناسب، و بدون عوارض جانبی به بدن رسانده شود. بیشتر اوقات، ویروسها به عنوان حامل ژن استفاده میشوند؛ چون بهطور طبیعی میتوانند وارد سلولها شوند. ولی ویروسهای معمولی تفاوتی بین سلول عضلانی و سلول کبدی نمیگذارند—هر سلولی را که بتوانند، آلوده میکنند. این عدم هدفگیری دقیق میتواند خطرناک باشد و کاربرد ژندرمانی را محدود کند.
تیمی از دانشمندان به رهبری دکتر داگلاس میلی راهحلی هوشمندانه پیشنهاد دادند:
"اگر بتوانیم ویروسهایی بسازیم که فقط سلولهای عضلانی را هدف بگیرند و سراغ هیچ بافت دیگری نروند، چه میشود؟"
در یک مطالعهی پیشگامانه که در مجله Cell در سال ۲۰۲۳ منتشر شد، این محققان موفق شدند ویروسی طراحی کنند که با استفاده از فرآیند طبیعی "جوش خوردن سلولهای عضلانی"، فقط وارد عضلات میشود.
مفاهیم پایه: چگونه سلولهای عضلانی به هم جوش میخورند؟
در طول رشد و ترمیم عضلات، سلولهای عضلانی (میوبلاستها) باید با هم ترکیب شوند تا فیبرهای عضلانی بزرگ و چندهستهای به نام میوفیبر تشکیل دهند. این فرآیند برای ساخت و نگهداری عضله ضروری است. دو پروتئین کلیدی در این فرآیند نقش دارند:
- Myomaker
- Myomerger (که به آن Myomixer یا Minion هم میگویند)
این دو پروتئین در غشای سلولهای عضلانی قرار دارند و به آنها کمک میکنند تا به هم جوش بخورند. آنها فقط در زمان رشد یا ترمیم عضله فعال هستند، به این معنی که در عضلات سالم و بیتحرک وجود ندارند.
محققان از خود پرسیدند:
"اگر این پروتئینها در جوش دادن غشاها اینقدر خوب عمل میکنند، آیا میتوان از آنها کمک گرفت تا ویروسها هم فقط با سلولهای عضله جوش بخورند؟"
آزمایش: دادن "هویت عضلانی" به ویروسها
ویروسها برای ورود به سلولها نیاز به پروتئینهای خاصی به نام فیوژنها (fusogens) دارند. این پروتئینها مانند ابزارهایی هستند که ویروس با استفاده از آنها غشای خودش را با غشای سلول میزبان ترکیب میکند.
ویروسهایی که امروزه در ژندرمانی استفاده میشوند (مانند لنتیویروس یا AAV) معمولاً از فیوژنهای ویروسی مثل VSV-G (از ویروس استوماتیت وزیکولار) استفاده میکنند. اما این پروتئینها غیر اختصاصی هستند و به ویروس اجازه میدهند هر نوع سلولی را آلوده کند.
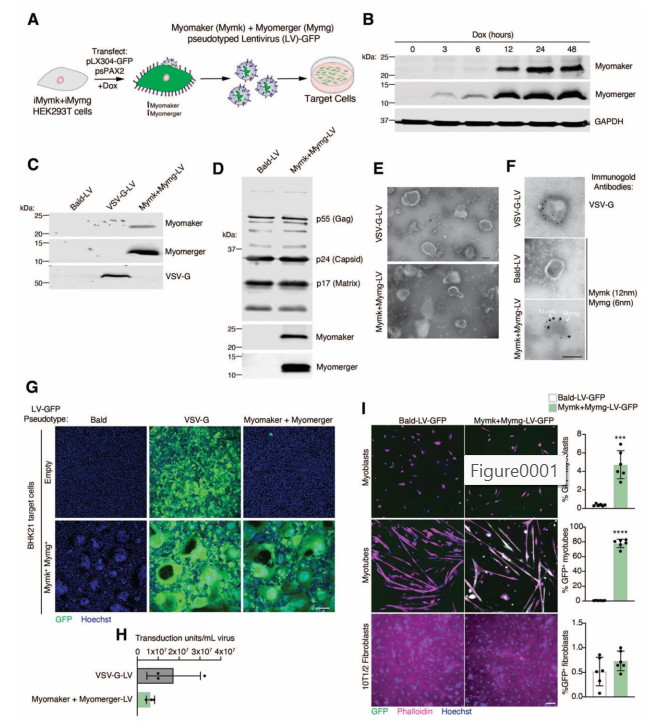
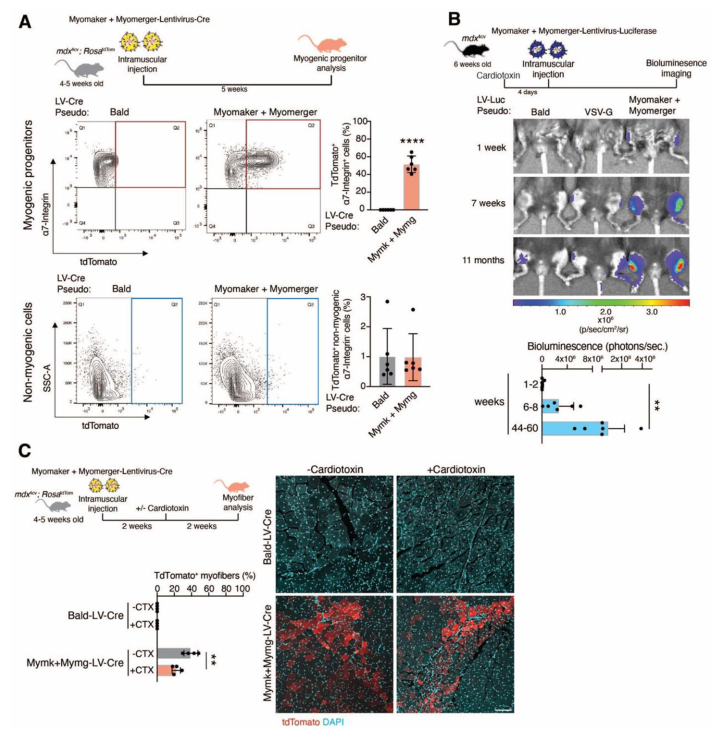
برای رفع این مشکل، تیم تحقیقاتی، فیوژن ویروسی را با پروتئینهای عضلانی Myomaker و Myomerger جایگزین کرد. آنها ویروس را طوری مهندسی کردند که این دو پروتئین روی سطح آن قرار بگیرند. به این فرآیند "سودوتایپینگ (pseudotyping)" میگویند؛ یعنی دادن یک ویژگی هدفگیری جدید به ویروس.
در نتیجه، این ویروسهای جدید فقط میتوانند با سلولهایی که Myomaker و/یا Myomerger دارند جوش بخورند—و همانطور که گفتیم، این سلولها عمدتاً سلولهای عضله در حال ترمیم هستند.
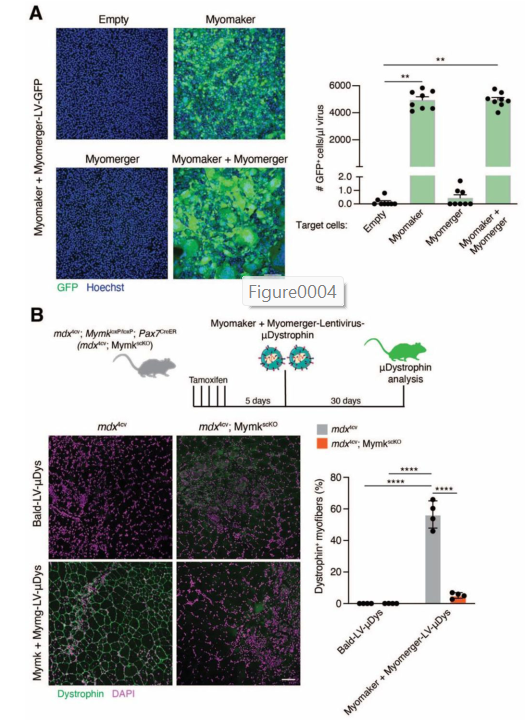
در آزمایشهای اولیه در محیط آزمایشگاه (in vitro):
- فقط توانستند وارد سلولهای عضلانی در حال ادغام شوند.
- وارد سلولهای غیرعضلانی مثل فیبروبلاستها نشدند.
این اولین نشانه امیدبخش از موفقیت این ایده بود.
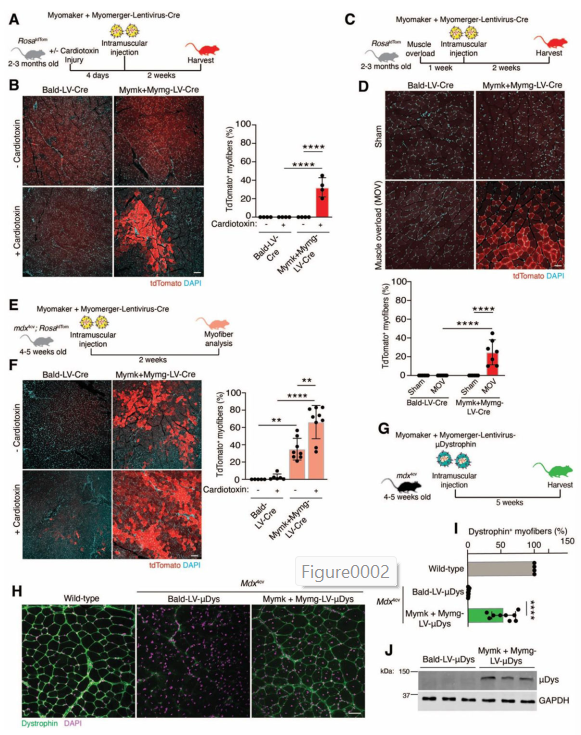
آزمایش در موشهای دیستروفی عضلانی
در مرحله بعد، محققان آزمایش را روی حیوانات زنده آغاز کردند. آنها از موشهای mdx4cv استفاده کردند که مدلی رایج برای بیماری دیستروفی عضلانی دوشن است. این موشها دیستروفین ندارند و مشکلات عضلانی مشابه انسانها در این بیماری را نشان میدهند.
محققان نسخهای کوچکشده از ژن دیستروفین به نام μDys (میکرودیستروفین) را داخل ویروس قرار دادند—این نسخه با اینکه کوچکتر از ژن کامل است، اما همچنان میتواند عملکرد لازم را داشته باشد.
سپس این ویروسها به دو روش تزریق شدند:
- تزریق مستقیم به عضله (مثلاً در پای موش)
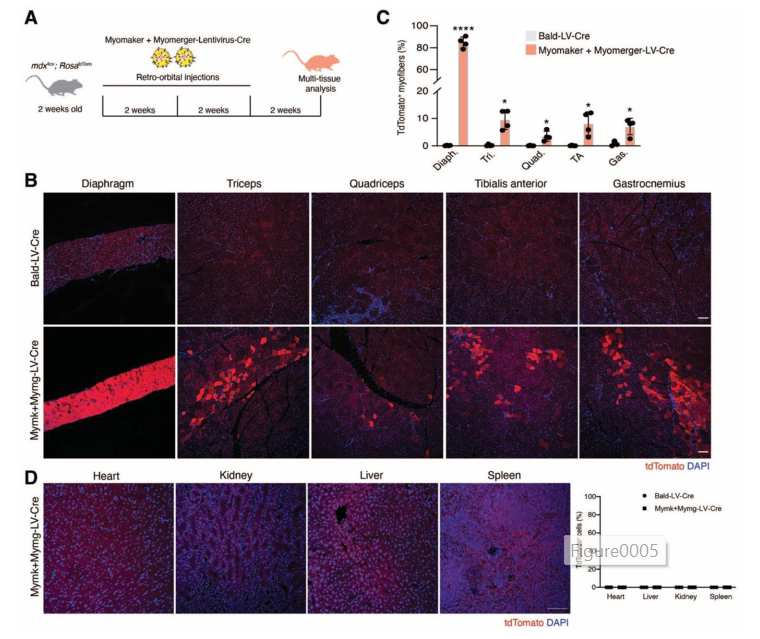
- تزریق از راه جریان خون (تزریق سیستمیک)
نتایج چه بود؟
- ✅ در عضلاتی که در حال ترمیم بودند (مثلاً بعد از آسیب یا در اثر بیماری)، ویروس توانست وارد سلولها شود و ژن را منتقل کند.
- ✅ در عضلات سالم و بدون آسیب، که پروتئینهای فیوژن فعال نبودند، ویروس عملاً اثری نداشت.
- ✅ مهمتر از همه، ویروس فقط به عضلهها رفت و وارد بافتهای دیگر مثل قلب یا کبد نشد.
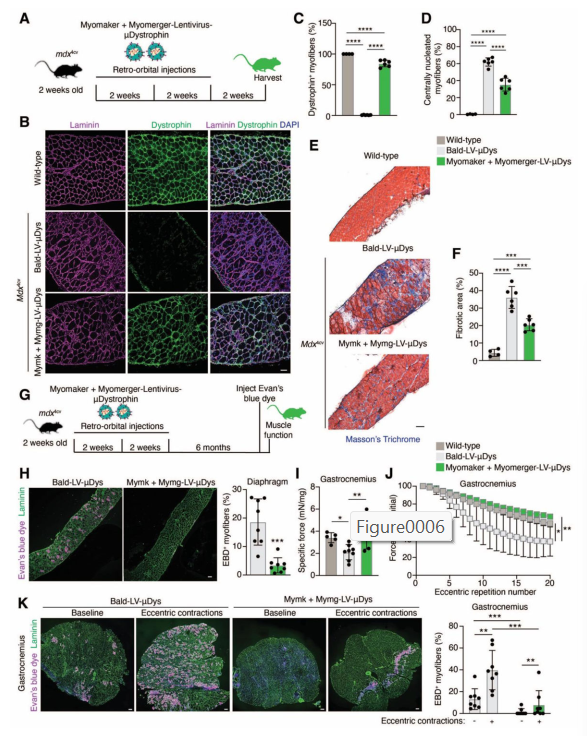
نتایج واقعی: بازگشت دیستروفین در عضلات
پس از تزریق ویروس، محققان بررسی کردند که آیا سلولهای عضلانی واقعاً شروع به تولید دیستروفین کردهاند یا نه.
- در تزریقهای موضعی، تعداد زیادی از تارهای عضلانی دیستروفین را تولید کردند.
- در تزریقهای سیستمیک، تا ۹۰٪ از تارهای عضلانی دیافراگم ژن میکرودیستروفین را بیان کردند.
- عضلات تحت درمان، کمتر دچار فیبروز شدند، کمتر آسیب دیدند و قدرت بیشتری داشتند.
حتی بعد از ۶ ماه از درمان، سطح دیستروفین همچنان بالا بود و عملکرد عضله حفظ شده بود.
آیا میتوان از این ویروس چند بار استفاده کرد؟
یکی از مشکلات بزرگ ژندرمانی با ویروسها این است که بدن بعد از اولین تزریق، آنها را شناسایی میکند و دفع میکند. بنابراین معمولاً نمیتوان از یک نوع ویروس چند بار برای درمان استفاده کرد.
اما در کمال تعجب، این ویروس مهندسیشده پاسخ ایمنی شدید ایجاد نکرد. محققان توانستند آن را چند بار به موشها تزریق کنند و در هر بار، ویروس عملکرد بهتری داشت.
در واقع، با سه نوبت تزریق، نزدیک به ترمیم کامل در عضله دیافراگم به دست آمد—نتیجهای بیسابقه در مطالعات مشابه.
چرا این روش یک تحول بزرگ است؟
- ✅ هدفگیری دقیق: ویروس فقط وارد سلولهای عضلانی فعال میشود— و نه سلولهای دیگر.
- ✅ تحویل ژن به مکان صحیح: بیماریهای عضلانی مانند دوشن شامل تخریب و ترمیم مداوم عضله هستند. این ویروس دقیقاً همان سلولهایی را هدف میگیرد که درگیر ترمیماند.
- ✅ قابل استفاده دوباره: بر خلاف ویروسهای معمولی، این ویروس میتواند چند بار استفاده شود.
- ✅ اثر طولانیمدت: عضلات بعد از درمان قویتر شدند و برای ماهها عملکرد خوبی داشتند.
- ✅ قابل استفاده برای ژنهای دیگر: این روش فقط محدود به دیستروفین نیست—میتوان هر ژن درمانی دیگری را نیز با این روش به عضله رساند.
محدودیتها و قدمهای بعدی
با اینکه نتایج بسیار امیدوارکننده است، هنوز سؤالاتی باقیمانده:
- آیا در انسان نیز جواب میدهد؟ این پژوهش فعلاً فقط روی موش انجام شده است.
- چه میشود اگر بخواهیم قلب را نیز هدف بگیریم؟ ویروس فعلی فقط عضلههای اسکلتی را هدف میگیرد.
- آیا در درازمدت ایمن است؟ چون لنتیویروسها وارد ژنوم سلول میشوند، خطر کمی برای ایجاد جهش یا سرطان وجود دارد.
با این حال، محققان معتقدند این ویروس میتواند همراه با سایر روشها، مانند AAV (برای هدفگیری قلب)، استفاده شود تا درمانی کاملتر ارائه دهد.
نتیجهگیری: عصر جدیدی در ژندرمانی عضله
این مطالعه یک گام مهم در مسیر ژندرمانی هدفمند است. با استفاده از پروتئینهایی که خود بدن برای جوش خوردن سلولهای عضلانی استفاده میکند، دانشمندان ویروسی ساختند که دقیقاً به جایی میرود که باید برود.
در آینده، این فناوری میتواند به درمانهای شخصیسازیشده، کارآمدتر و ایمنتر برای انواع بیماریهای عضلانی منجر شود—نه فقط دوشن.
آیندهی ژندرمانی عضله، روشنتر از همیشه است.








| Field | Details |
|---|---|
| Title | Enveloped viruses pseudotyped with mammalian myogenic cell fusogens target skeletal muscle for gene delivery |
| Authors | Sajedah M. Hindi, Michael J. Petrany, Elena Greenfeld, Leah C. Focke, Alyssa A. W. Cramer, Michael A. Whitt, Ramzi J. Khairallah, Christopher W. Ward, Jeffrey S. Chamberlain, Vikram Prasad, Benjamin Podbilewicz, Douglas P. Millay |
| Corresponding Author | Douglas P. Millay (douglas.millay@cchmc.org) |
| Publication Date | May 11, 2023 (final) / Available in PMC: June 17, 2024 |
| Journal | Cell |
| Keywords | Skeletal muscle, gene therapy, pseudotyped viruses, Myomaker, Myomerger, dystrophin delivery, Duchenne Muscular Dystrophy (DMD) |
| Methods Used | AAV/lentiviral pseudotyping, in vivo gene delivery, histology, RT-qPCR, western blot, functional muscle tests in mdx mice |
| Study Type | Preclinical gene delivery platform development in mouse model |
| DOI | 10.1016/j.cell.2023.03.033 |