حذف شرطی دیستروفین: دریچهای به درک عمیقتری از رشد عضله و عملکرد عصبی
دیستروفین: پروتئینی کلیدی در سلامت عضله
دیستروفین یکی از حیاتیترین پروتئینها برای حفظ ساختار و عملکرد صحیح عضله است. نبود یا اختلال در این پروتئین، علت اصلی بیماریهای ناتوانکنندهای مانند دیستروفی عضلانی دوشن (Duchenne Muscular Dystrophy - DMD) است. این بیماری پیشرونده و ژنتیکی، به مرور زمان موجب ضعف شدید عضلانی، ناتوانی حرکتی و در نهایت مرگ زودهنگام میشود. بیشتر مطالعات قبلی تمرکز خود را بر حذف کامل دیستروفین از بدن قرار دادهاند، اما اثرات دقیق حذف انتخابی آن در بافت خاصی همچون عضله اسکلتی هنوز بهطور کامل بررسی نشده بود.
هدف این مطالعه چه بود؟
در این پژوهش پیشچاپی پیشگامانه، محققان به رهبری دکتر متیو الکساندر و دکتر لوئیس کانکل، با استفاده از مدلهای حیوانی، اثرات حذف شرطی (یعنی هدفمند و بافت-خاص) دیستروفین را در سلولهای ماهوارهای بررسی کردند. هدف آنها، فهم دقیقتر از نقش دیستروفین در مراحل مختلف رشد عضله، تعیین سرنوشت سلولهای بنیادی عضلانی، رفتار عصبی و تنظیم شبکههای ژنی مرتبط با ماتریکس خارجسلولی بود.
حذف شرطی دیستروفین در سلولهای بنیادی عضلانی
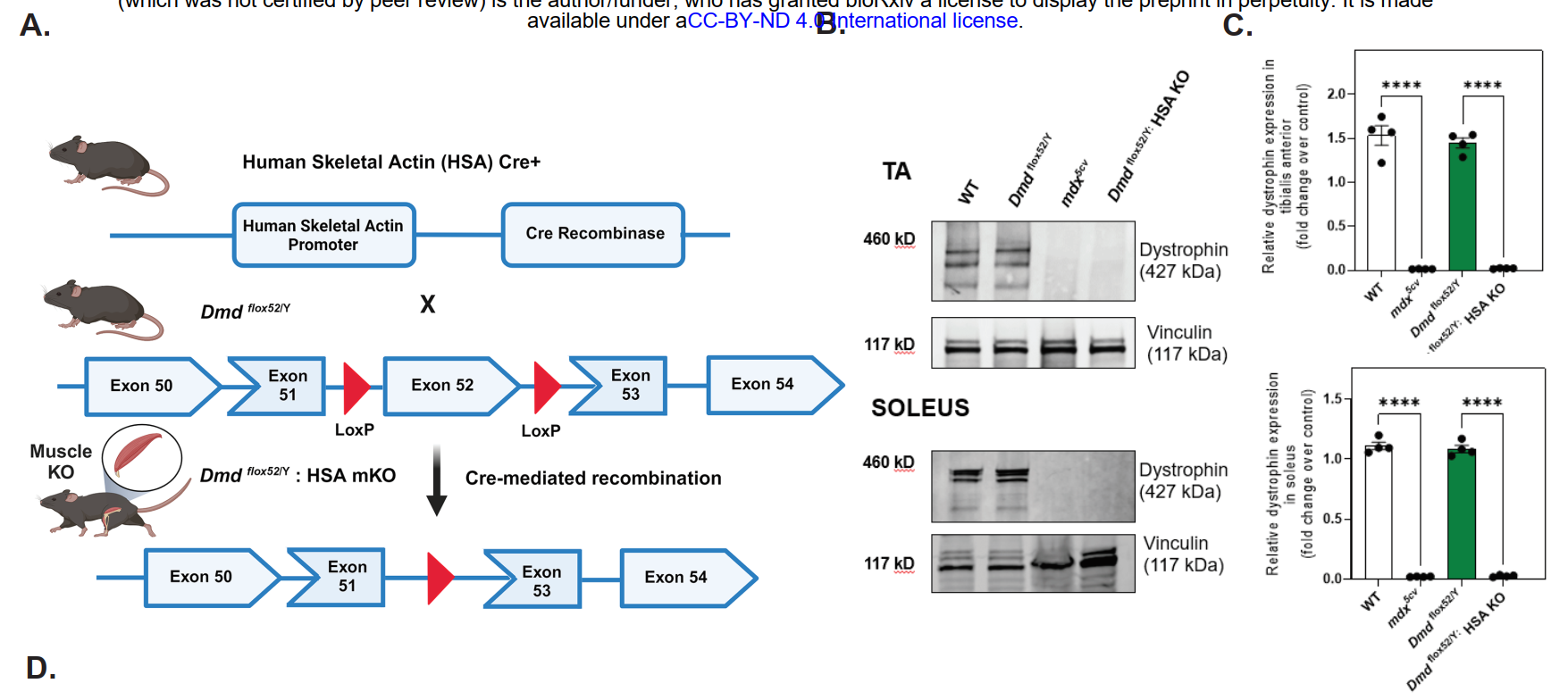
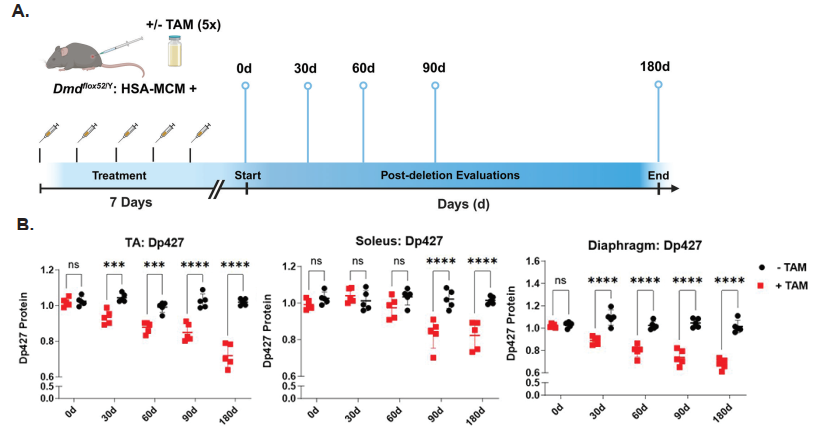
برای حذف دقیق دیستروفین از سلولهای بنیادی عضلانی (سلولهای ماهوارهای)، پژوهشگران از سیستم Cre-LoxP استفاده کردند. آنها موشهایی با آلل Dmd-flox تولید کردند و آن را با موشهایی که Cre را تحت پروموتر Pax7 بیان میکردند، تلاقی دادند. بدین ترتیب، حذف دیستروفین تنها در سلولهای ماهوارهای فعالشده اتفاق افتاد. این مدلها تحت عنوان scKO (satellite cell-specific knockout) شناخته شدند.
اثرات حذف دیستروفین بر رشد عضله
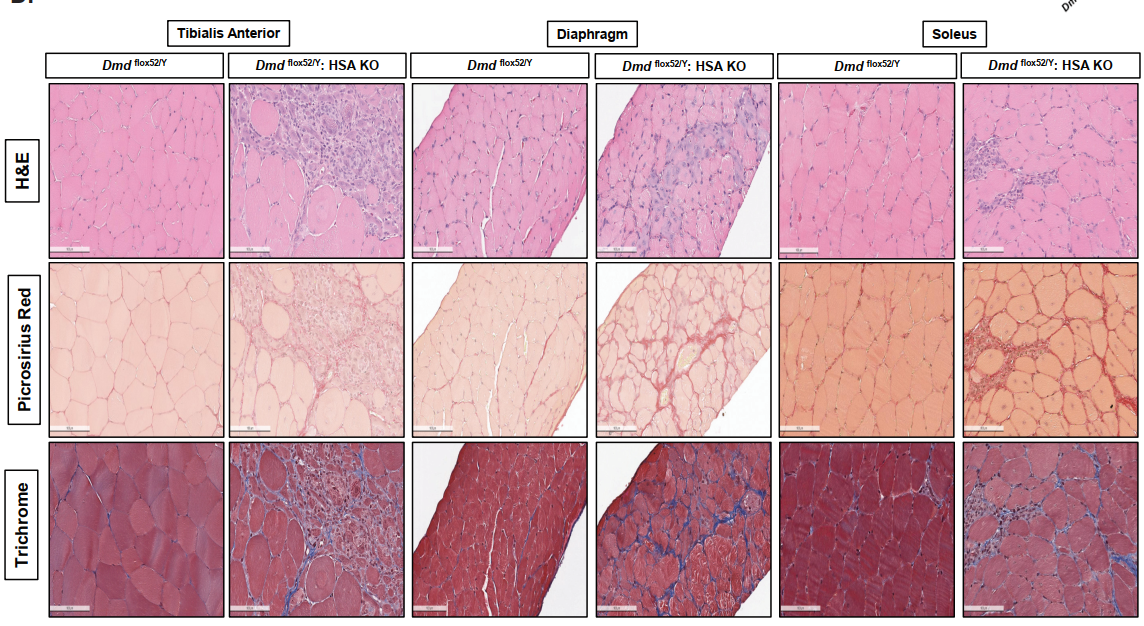
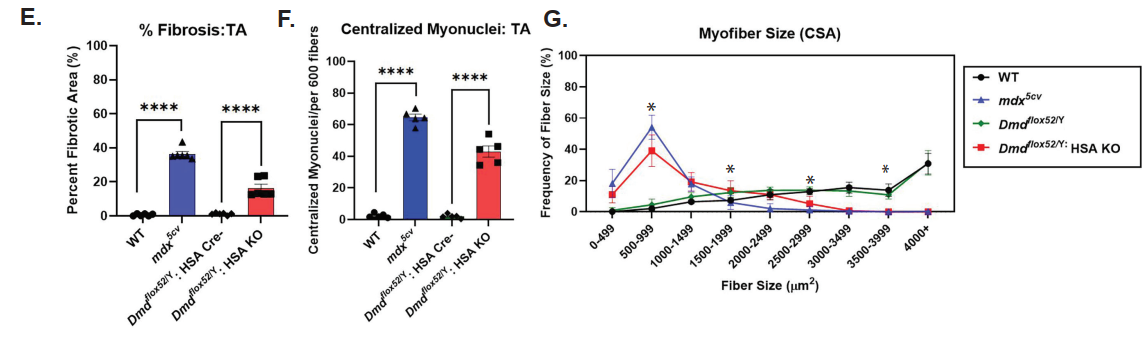
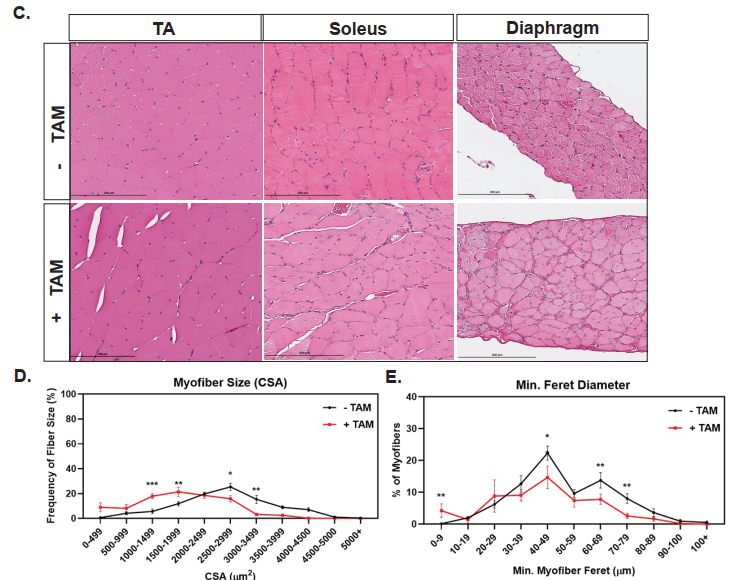
یکی از یافتههای کلیدی این مطالعه آن بود که موشهای scKO نسبت به کنترلها دچار اختلالات ساختاری شدیدی در عضلات اسکلتی شدند. تحلیلهای بافتشناسی نشان داد که این عضلات دارای اندازهی کوچکتر، افزایش فیبروز و هستههای مرکزی بیشتری بودند. همچنین، توانایی بازسازی عضله پس از آسیب، در این موشها بهطور قابل توجهی کاهش یافت. این نتایج نشان میدهد که دیستروفین نقش حیاتی نه تنها در عضله بالغ، بلکه در مراحل ابتدایی رشد و تنظیم سرنوشت سلولی ایفا میکند.
اختلال در تعیین سرنوشت سلولهای ماهوارهای
با استفاده از RNA-seq و تحلیلهای تکسلولی، پژوهشگران دریافتند که حذف دیستروفین موجب تغییر در مسیرهای ژنتیکی کلیدی مرتبط با تکامل سلولهای عضلانی میشود. سلولهای ماهوارهای در موشهای scKO به درستی به سمت سلولهای میوبلاست، میوسیت یا فیبر عضلانی تمایز پیدا نمیکردند. این اختلال در مسیرهای تفکیک سلولی احتمالاً عامل اصلی کاهش بازسازی عضله در این مدلها است.
تغییرات گسترده در ماتریکس خارجسلولی
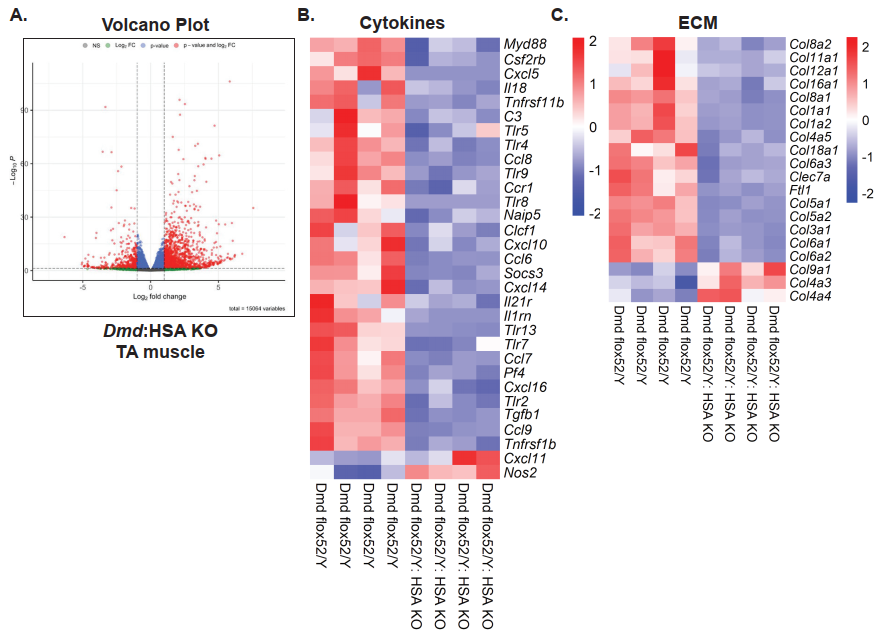
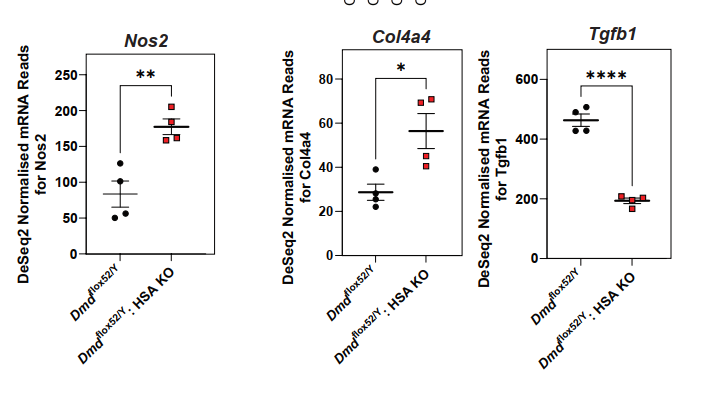
تحلیل مسیرهای بیان ژن نشان داد که حذف دیستروفین باعث افزایش بیان ژنهای مرتبط با ماتریکس خارجسلولی (ECM) میشود؛ از جمله کلاژنها، پروتئوگلیکانها و آنزیمهای مرتبط با بازسازی ECM. این افزایش میتواند زمینهساز فیبروز شدید عضلات و اختلال در ساختار بافتی باشد. بنابراین، دیستروفین نقش مهمی در تنظیم تعادل ECM ایفا میکند که فراتر از نقش ساختاری کلاسیک آن در غشای سلولی است.
اثرات نوروبیولوژیک: تغییر در رفتار و عملکرد شناختی
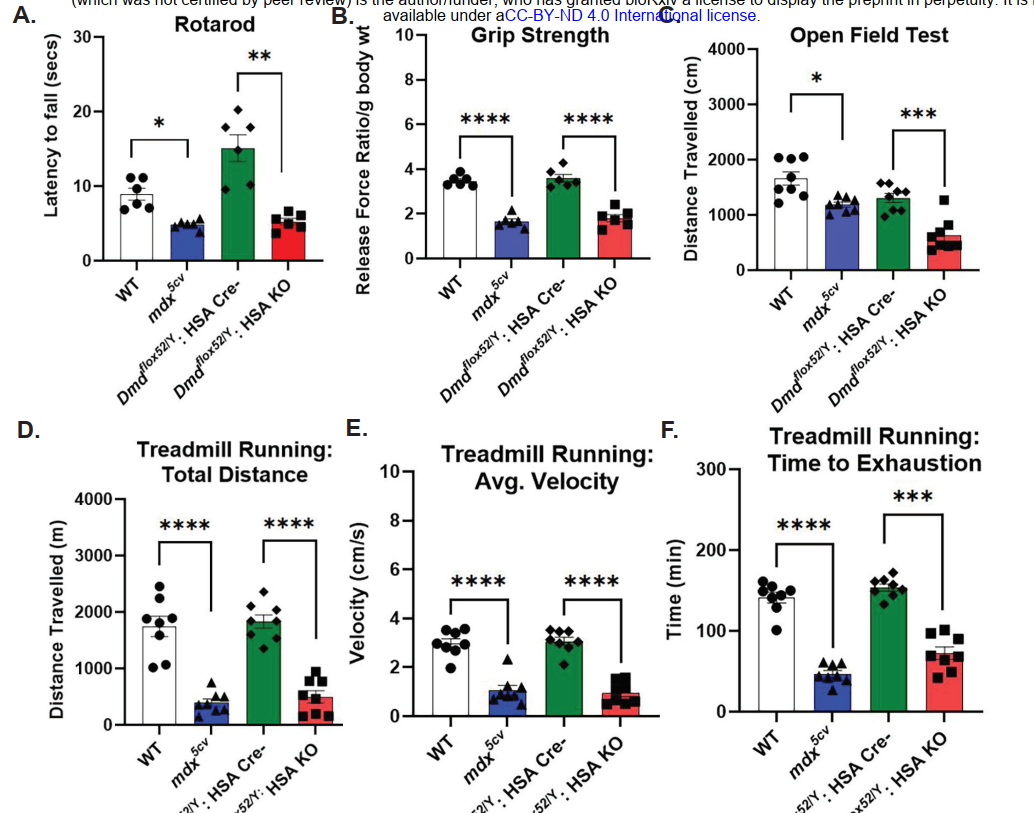
یکی از جنبههای برجستهی این مطالعه، بررسی اثرات حذف اختصاصی دیستروفین در بافتهای مختلف و پیامدهای رفتاری آن بود. در مدل scKO (یا Dmd mKO) که دیستروفین بهطور اختصاصی در عضلهی اسکلتی حذف شده بود، آزمونهای حرکتی و اضطرابی نشان دادند که این موشها فعالیت بدنی کمتری دارند، بیشتر در گوشهها و نواحی تاریک باقی میمانند و تمایل کمتری به کاوش محیط از خود نشان میدهند. اگرچه این مدل برای بررسی اثرات عضلانی دیستروفین طراحی شده بود، اما این تغییرات رفتاری احتمال وجود ارتباطهای عملکردی میان عضله و مغز را مطرح میکند، که میتواند از طریق مسیرهای سیگنالدهی محیطی یا تعاملات جنینی عضله با سیستم عصبی شکل بگیرد.
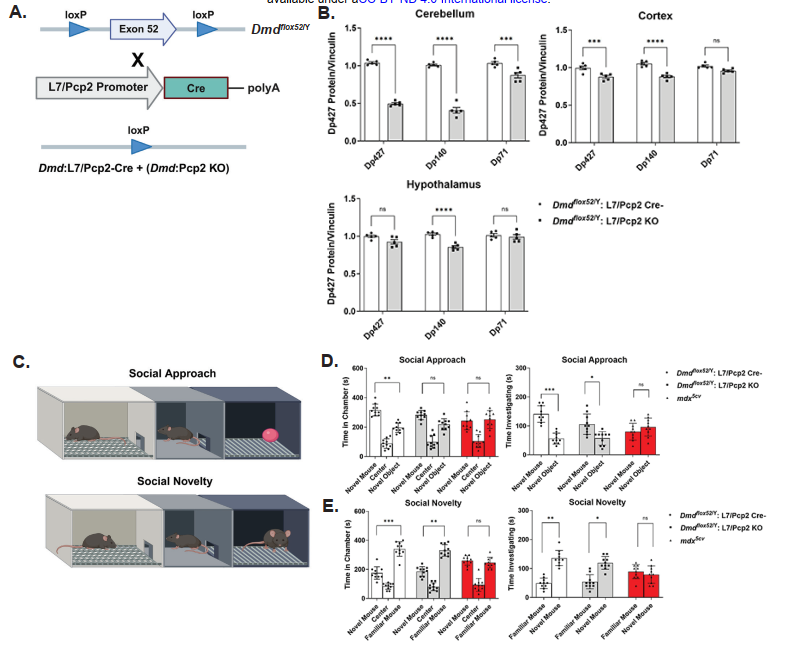
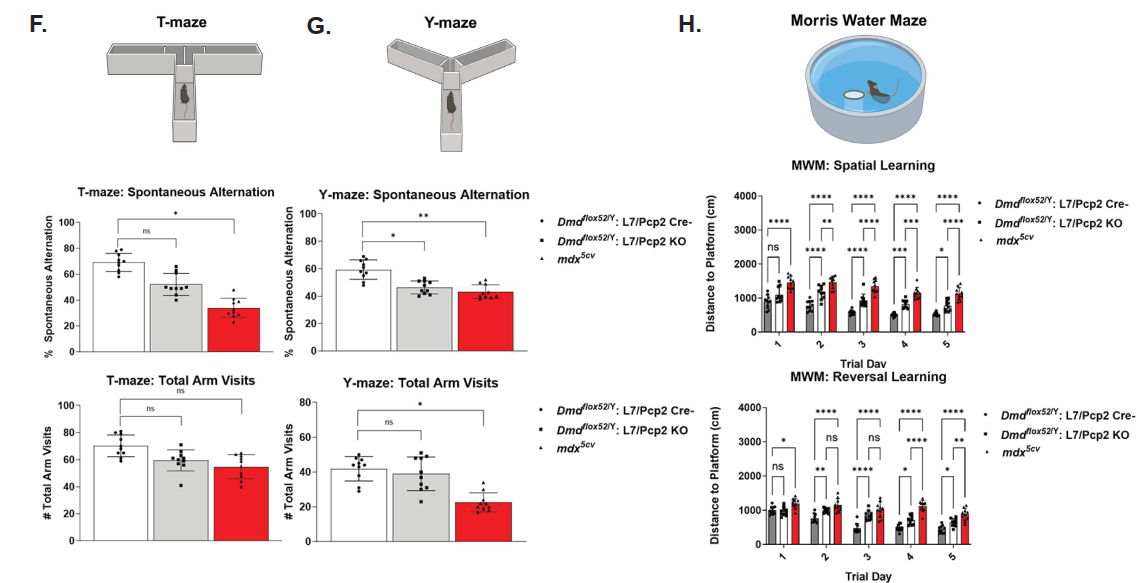
در مقابل، در مدل Dmd:Pcp2 KO که حذف دیستروفین بهطور اختصاصی در نورونهای پورکینژ مخچه انجام شد، نقصهای آشکار در عملکردهای نوروبیولوژیک شامل حافظهی کاری، شناخت فضایی، تعاملات اجتماعی و حافظه اجتماعی مشاهده شد. این یافتهها نشان میدهند که ایزوفرم مغزی دیستروفین (Dp427c) نقش حیاتی در تنظیم عملکردهای شناختی و رفتاری ایفا میکند. بنابراین، دیستروفین نه تنها برای حفظ ساختار و عملکرد عضله ضروری است، بلکه در مغز نیز برای عملکرد طبیعی نوروبیولوژیک حیاتی محسوب میشود.
تحلیلهای مولکولی: تقویت نتایج رفتاری و بافتی
تحلیلهای ژنبیانی (bulk RNA-seq و single-cell RNA-seq) نشان دادند که مسیرهای متعددی تحت تأثیر حذف دیستروفین قرار گرفتهاند. از جمله مسیرهای مرتبط با:
- تکامل عضله (Myod1, Myog)
- ECM remodeling (Col1a1, Col3a1, Mmp2)
- مسیرهای ایمنی (TGFβ signaling, interferon response)
- رفتارهای سلولی (migration, adhesion, differentiation)
همچنین، اختلال در بیان ژنهای مربوط به حافظه و یادگیری در مغز نیز در موشهای scKO مشاهده شد که بهخوبی با نتایج رفتاری همراستا بود.
جمعبندی: چرا این مطالعه مهم است؟
این پژوهش برای اولین بار نشان میدهد که حذف دیستروفین بهصورت بافت-اختصاصی در سلولهای بنیادی عضلانی، نه تنها باعث اختلال در رشد عضله میشود بلکه پیامدهای رفتاری و شناختی عمیقی نیز در پی دارد. این یافتهها دیدگاه ما را درباره نقش دیستروفین گسترش میدهند و آن را بهعنوان یک تنظیمکنندهی چندبعدی در مسیرهای رشد عضله، عملکرد ECM و حتی عملکرد شناختی معرفی میکنند.
چشمانداز آینده
بر اساس این یافتهها، میتوان پرسشهای مهمی را برای پژوهشهای آینده مطرح کرد:
- آیا حذف دیستروفین در زمانهای مختلف رشد (جنینی، نوجوانی، بلوغ) اثرات متفاوتی دارد؟
- نقش دقیق ارتباط عضله-مغز در ایجاد اختلالات شناختی چیست؟
- آیا میتوان با هدف قرار دادن ECM یا مسیرهای سیگنالدهی متأثر از دیستروفین، بخشی از اثرات منفی را کاهش داد؟
- آیا دیستروفین در سایر سلولهای بنیادی (غیر عضلانی) نیز عملکرد مشابهی دارد؟











| فیلد | جزئیات |
|---|---|
| عنوان مقاله | حذف شرطی دیستروفین باعث اثرات عمیق بر رشد عضله، رفتار عصبی و مسیرهای ماتریکس خارجسلولی میشود |
| نویسندگان | Muthukumar Karuppasamy، Katherine G. English، James R. Conner، Shelby N. Rorrer، Michael A. Lopez، David K. Crossman، Jodi R. Paul، Miguel A. Monreal-Gutierrez، Karen L. Gamble، Karyn A. Esser، Jeffrey J. Widrick، Louis M. Kunkel، Matthew S. Alexander |
| نویسنده مسئول | Matthew S. Alexander (matthewalexander@uabmc.edu) |
| تاریخ انتشار | ۱ فوریه ۲۰۲۵ (پیشچاپ در bioRxiv) |
| ژورنال | bioRxiv (پیشچاپ) |
| کلیدواژهها | Dystrophin، دیستروفی عضلانی دوشن (DMD)، عضله اسکلتی، دیستروفینوپاتی |
| روشهای بهکاررفته | ویرایش ژن با CRISPR/Cas9، ایجاد موشهای Knockout شرطی، رنگآمیزی بافتی (H&E، تریکرو، پیکروسیریوس رد)، ایمونوفلورسانس، وسترن بلات، آزمونهای عملکرد عضله، آزمونهای رفتاری (rotarod، grip strength، Morris water maze)، RNA-seq، qPCR |
| نوع مطالعه | مطالعه پیشبالینی عملکرد اختصاصی ژنی در مدلهای موشی شرطی |
| شناسه DOI | 10.1101/2025.01.30.635777 |














